Tour d’horizon sur les médicaments

De nombreuses personnes se rendent régulièrement à la pharmacie pour acheter des médicaments. Vous vous êtes peut-être déjà demandé par quel processus passe un médicament avant d'être disponible en pharmacie? Comment un médicament est-il développé? Et qu'en est-il des effets indésirables?
Ce tour de connaissances vous donne différentes informations sur les médicaments - recherche et développement, avantages et risques, notice d'emballage et sécurité des médicaments - ainsi que des conseils pour comprendre les statistiques.
De la molécule au médicament

Cela prend environ 10 à 16 ans avant qu’un médicament ne soit autorisé. Durant cette période, les scientifiques et les médecins examinent en détails le principe actif: en laboratoire, sur des volontaires sains et des milliers de patients participant aux études cliniques de façon volontaire.
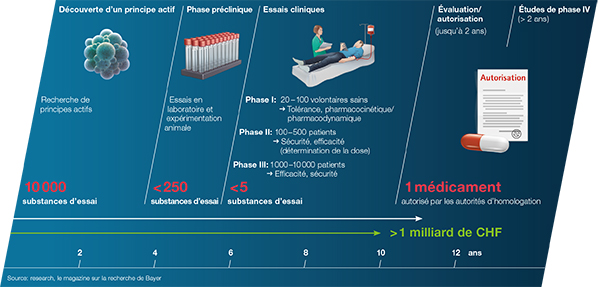
Sur environ 10 000 substances évaluées en détails, il n’y a en règle générale qu’un seul principe actif qui fera l’objet d’une demande d’autorisation. Les autorités de santé, Swissmedic pour la Suisse, évaluent les nombreuses données obtenues lors du développement préclinique et clinique. Ce n'est qu’une fois que Swissmedic autorise le médicament qu’il est disponible pour les patients.

Vous trouverez de plus amples informations sur le développement des médicaments dans la brochure (en anglais)
« From Molecules To Medicine » (PDF, 3,6 MB).
Vous trouverez de plus amples informations sur l’autorisation des médicaments en Suisse sur les sites Internet de Swissmedic et d'Interpharma.
Prix, remboursement et protection contre la copie des médicaments

Une fois autorisés, les médicaments ne sont pas automatiquement pris en charge par l’assurance de base. Seuls les médicaments figurant sur la liste des spécialités sont remboursés. C’est l’Office fédéral de la santé publique qui décide de l’admission des médicaments dans la liste des spécialités et de leur prix. L’autorité fixe les prix des médicaments et les contrôle régulièrement.
Pour la fixation des prix, l’Office fédéral de la santé publique effectue une comparaison thérapeutique (CT, comparaison transversale avec des produits équivalents sur le plan thérapeutique, déjà autorisés pour la même maladie) et une comparaison de prix avec les pays étrangers (CPE, comparaison avec les prix pratiqués en Belgique, au Danemark, en Allemagne, au Royaume-Uni, en Finlande, en France, aux Pays-Bas, en Autriche et en Suède). La CT et la CPE sont prises en compte à égalité.
Vous recevrez de plus amples informations à ce sujet sur le site Internet d’Interpharma. Vous trouverez ici la liste des spécialités, c’est-à-dire la liste sur laquelle figurent tous les médicaments admis par les caisses-maladie en Suisse.

Les brevets sont une incitation indispensable à investir dans la recherche et le développement de nouveaux produits et technologies. Une protection limitée dans le temps contre l'imitation sert à tous : L'investissement peut être rentabilisé et l'innovation peut être utilisée par tous après l'expiration de la période de protection.
La durée légale du brevet est de 20 ans et commence au moment du dépôt du brevet – en général avant la phase préclinique. En cas d'autorisation de mise sur le marché, la protection par brevet ne dure en moyenne plus que huit ans. Après l'expiration du brevet, des produits d'imitation, appelés génériques, peuvent être mis sur le marché.
 Fiche d'information "4 choses que vous ne savez peut-être pas encore à propos des brevets" (PDF, 158 KB).
Fiche d'information "4 choses que vous ne savez peut-être pas encore à propos des brevets" (PDF, 158 KB).
Vous trouverez de plus amples informations à ce sujet sur le site Internet d’Interpharma.
Faits sur les bénéfices et les risques

Un médicament peut ne pas entraîner que des effets désirables dans le corps, mais aussi des effets indésirables. Pour cette raison, les médicaments sont rigoureusement testés et uniquement autorisés par les autorités de santé s’ils sont efficaces et bien tolérés.
Les entreprises pharmaceutiques investissent la majeure partie des coûts de développement, s’élevant à plus d’un milliard de francs suisses par médicament, dans l’évaluation clinique de l'efficacité et de la tolérance d'un principe actif.
Les bénéfices et les risques continuent à être analysés et évalués après l’autorisation. L’efficacité du médicament est alors souvent évaluée dans la pratique quotidienne «réelle». Les résultats tirés de ces observations sont souvent qualifiés de «données en vie réelle».
Des études cliniques réalisées avec des groupes de patients souvent sélectionnés de façon restrictive montrent qu’une préparation «peut avoir un effet». Après l’autorisation, la question de savoir comment le médicament agit chez les différents patients du monde «réel» subsiste. Les données en vie réelle permettent de répondre à cette question car elles rendent compte des résultats d’un traitement dans la population générale.
Les données en vie réelle complètent le profil d’un médicament en approfondissant les connaissances relatives à l’efficacité, à la sécurité et aux coûts dans des conditions pratiques sans restriction:
| Étude clinique | Données en vie réelle | |
|
Cadre exactement prédéfini |
Environnement thérapeutique |
Conditions pratiques «réelles» |
|
Contrôlée (p. ex par rapport à un placebo)
Randomisée (assignation des patients au hasard dans le groupe avec le principe actif ou sous placebo)
En aveugle (ni le médecin ni le patient ne connaissent la répartition) |
Conditions d’étude |
«En ouvert», sans restriction |
| Homogène (sélection des patients en fonction de certains critères, p. ex. pas de traitement préalable, catégorie d’âge définie) |
Patients |
Hétérogènes (aucun critère de sélection, tous les patients peuvent être inclus) |

Informations destinées aux patients au sujet d'un médicament

La notice d’emballage fournit des informations sur les domaines d’utilisation (appelés indications), la posologie, les effets, les éventuels interactions et effets indésirables ainsi que les précautions. Les effets indésirables en rapport avec l’utilisation d’un médicament et les interactions avec d’autres médicaments que les médecins ont observé durant l’étude clinique et après l’autorisation doivent être listés dans la notice d’emballage. C’est pour cette raison qu’une notice d’emballage peut être considérée comme étant détaillée.
Les notices d’emballage suivent un schéma uniforme imposé par les autorités de santé. Les autorités vérifient et approuvent les notices d’emballage. Toutes les notices d’emballage sont régulièrement vérifiées et adaptées pour refléter l’état actuel de la recherche scientifique. Les informations suivantes vous donnent des indications importantes sur l’utilisation des médicaments.
Information n° 1
Veuillez vous conformer au dosage figurant sur la notice d’emballage ou prescrit par votre médecin.
La posologie, c’est-à-dire la quantité de médicament et la fréquence à laquelle vous devez le prendre avant, pendant ou après un repas, a été déterminée dans des études spéciales de détermination de la dose ainsi que dans des études cliniques avec des centaines voire des milliers de patients.
À la posologie optimale, les effets désirables et éventuels effets indésirables ont un rapport favorable. Une modification de la posologie effectuée de votre propre chef peut nuire à l’effet du médicament et augmenter le risque d’effets indésirables.
Information n° 2
Lisez soigneusement les sections sur les restrictions d’emploi, les précautions et les effets indésirables.
Les sections en question expliquent quand vous ne devez pas, ou uniquement sous surveillance médicale, utiliser le médicament, par exemple si vous êtes allergique à l’un des composants, si vous souffrez d’insuffisance hépatique ou rénale, si vous prenez certains autres médicaments en même temps ou si vous êtes enceinte.
Si vous avez des questions concernant la notice d’emballage, discutez-en avec votre médecin ou votre pharmacien.
Information n° 3
Prenez la date de péremption et les informations concernant le stockage au sérieux.
Quand le lait tourne, on peut le sentir. En revanche, un médicament trop vieux ou qui a mal été stocké a souvent toujours la même apparence. Il peut cependant avoir perdu son effet ou ne plus être bien toléré lors de son utilisation.
Lorsque vous achetez un nouveau médicament, respectez les informations concernant le stockage figurant dans la notice d’emballage ou sur l’emballage. Et avant de le prendre, assurez-vous que le médicament n’est pas périmé en vérifiant la date de péremption sur l’emballage. N’utilisez pas les médicaments lorsqu’ils sont périmés ou si vous ne savez pas s’ils ont été correctement stockés. En cas de doute, montrez le médicament à votre pharmacien et demandez-lui conseil.
Information n° 4
Informez-vous sur les effets indésirables qu’un médicament peut avoir.
La notice d’emballage liste les effets indésirables et mentionne à quelles fréquences ils ont été observés. «Fréquent» signifie: chez un sur dix à un sur 100 patients. Les effets indésirables «très rares» concernent moins d’un patient sur 10 000.
Lorsque vous prenez un médicament, soyez attentifs à l’éventuelle survenue de l’un des effets indésirables mentionnés ou d’une autre réaction inhabituelle. Si vous ressentez une quelconque dégradation de votre bien-être pendant ou après la prise d’un médicament, demandez conseil à votre médecin ou votre pharmacien dans les plus brefs délais.
Interprétation des chiffres sur les bénéfices et les risques

Les données statistiques et en particulier les chiffres en apparence élevés concernant le risque d’un événement indésirable peuvent être déroutants. Un risque décrit la possibilité qu’un événement indésirable survienne. Cela n’indique en rien que cet événement va se manifester chez vous.
Le contexte est important pour évaluer les chiffres de façon correcte. Et: tous les gros titres accrocheurs concernant les médicaments ne sont pas basés sur des faits avérés. Deux exemples.
Exemple 1
Les données cliniques montrent que le risque est de 50% plus élevé chez les femmes que chez les hommes.
Cela dépend. La phrase compare les risques de deux groupes de personnes. Elle ne dit pas combien d’hommes et de femmes sont effectivement concernés. Si la phrase se réfère par exemple à trois femmes et deux hommes d’un groupe de deux millions de personnes, le danger est relativement faible.
Exemple 2
Statistiquement, l'effet secondaire survient chez 20% de tous les patients traités par le médicament.
La phrase dit: l’effet secondaire survient chez 20 personnes sur 100 qui prennent le médicament. Si vous utilisez le médicament, votre risque s’élève à 1 sur 5. Dans le monde de l’évaluation du risque, c’est un chiffre relativement élevé. Néanmoins: l’effet secondaire ne se manifeste pas chez la grande majorité des patients de cet exemple, soit 80%.
De la posologie aux effets indésirables

Trouver le meilleur schéma de prise du médicament fait partie de son développement. La notice d’emballage indique la posologie recommandée (par exemple un comprimé trois fois par jour).
Modifier la posologie de son propre chef comporte des risques. L’effet du médicament peut être diminué et le risque d’effets indésirables peut éventuellement être augmenté. Si vous avez des difficultés à prendre le médicament tel que prescrit, parlez-en à votre médecin. Il sait ce qu’il faut faire et pourra peut-être vous prescrire un autre médicament.

Les effets indésirables ne peuvent pas être complètement évités. Veuillez contacter votre médecin ou votre pharmacien dans les plus brefs délais si vous pensez souffrir d’un effet indésirable. Ils sont les seuls à pouvoir vous conseiller de façon compétente et le cas échéant à pouvoir adapter le traitement ou la posologie.
Votre médecin et votre pharmacien sont tenus d’annoncer les effets secondaires à l’autorité de santé, Swissmedic en Suisse. Les cas signalés sont soigneusement examinés. Il est possible que l’information se retrouve ensuite dans la notice d’emballage. Les patients peuvent eux aussi annoncer des effets indésirables.
Si vous souhaitez annoncer un effet secondaire ou adresser une réclamation concernant la qualité, veuillez contacter votre médecin, votre pharmacien ou Swissmedic.
 Pour en apprendre davantage au sujet de la sécurité des patients au sein de l’entreprise Bayer et savoir comment vous pouvez y contribuer, consultez notre brochure «Notre responsabilité en matière de sécurité des patients» (PDF 539 KB).
Pour en apprendre davantage au sujet de la sécurité des patients au sein de l’entreprise Bayer et savoir comment vous pouvez y contribuer, consultez notre brochure «Notre responsabilité en matière de sécurité des patients» (PDF 539 KB).
Faits concernant les médicaments de contrefaçon et leurs risques

Il n’est pas rare que les médicaments de contrefaçon soient fabriqués par des criminels professionnels et distribués par des fournisseurs en ligne illégaux. Les copies de médicaments ressemblent parfois à s’y méprendre au produit original. Les dangers pour votre santé sont cependant importants: les comprimés de contrefaçon ne contiennent peut-être pas de principe actif ou au contraire une dose incorrecte, d’autres composants que ceux indiqués, voire même des substances toxiques.
La meilleure protection contre ces contrefaçons: n’achetez vos médicaments que chez un fournisseur digne de confiance. Si vous n’êtes pas sûr si le médicament est un original ou une contrefaçon, ne l’utilisez en aucun cas. Remettez-le plutôt à votre médecin ou votre pharmacien, aux autorités de santé ou au fabricant pour qu’il puisse être examiné.
Vous trouverez de plus amples informations sur les sites web d’Interpharma ou de l'association d'utilité publique STOP À LA PIRATERIE.
Check-list pour votre prochain rendez-vous chez le médecin

Cela vaut la peine de préparer son entretien avec son médecin. La check-list suivante vous permet d’avoir les points les plus importants à portée de main. Préparez au préalable des notes pour discuter de tous les points avec votre médecin. Prenez également des notes durant la consultation pour éviter d’oublier des informations importantes.
Vous pouvez remplir la check-list directement en ligne puis l’imprimer ou la télécharger et remplir vos notes à la main. Pour des raisons de protection des données, vos entrées ne seront pas enregistrées.

Télécharger la check-list (PDF)
PP-OTH-CH-0074-1 2410


